NIEDERMOLEKULARE HEPARINE: UNTERSCHIEDLICHER ZULASSUNGSSTATUS |
Ihren Artikel "Fondaparinux (ARIXTRA) bei Lungenembolie nicht besser als unfraktioniertes Heparin" (a-t 2003; 34: 103) haben wir mit Interesse gelesen. ... Der letzte Satz dieses Artikels könnte dahingehend
missverstanden werden, dass Certoparin (MONO EMBOLEX), Enoxaparin (CLEXANE), Nadroparin (FRAXIPARIN, FRAXODI) und Tinzaparin (INNOHEP) alle eine
gleiche Zulassung zur Therapie venöser Thromboembolien besitzen. Tatsächlich sind Certoparin, Enoxaparin und Nadroparin zur "Therapie tiefer
Venenthrombosen" zugelassen. Tinzaparin (INNOHEP 20.000 Anti-Xa I.E./ml) hingegen hat als einziges
niedermolekulares Heparin die Zulassung"zur Behandlung von Venenthrombosen und thromboembolischen Erkrankungen, einschließlich tiefer
Venenthrombosen und Lungenembolien" (Hervorhebungen durch Red.). Die mindestens genauso gute Wirksamkeit und Sicherheit wie
unfraktioniertes Heparin zur Therapie der akuten Lungenembolie hat Tinzaparin in einer großen randomisierten Studie1 bewiesen. ...
Dr. rer. nat. P. HENNE (Leo Pharma GmbH)
D-63263 Neu-Isenburg
Interessenkonflikt: Mitarb. des Herstellers von Tinzaparin (INNOHEP)
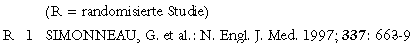
Das Bundesinstitut für Arzneimittel und Medizinprodukte nimmt auf Anfrage dazu Stellung:
... Laut den aktuellen Zulassungsanforderungen1 müssen separate Daten für Patienten mit tiefen Beinvenenthrombosen bzw. mit
Lungenembolie erhoben werden und die Wirksamkeit eines neuen Mittels muss in beiden Patientenkollektiven gezeigt werden (sofern die Lungenembolie als
Indikation beansprucht wird)... Der unterschiedliche Zulassungsstand der niedermolekularen Heparine entspricht also exakt der jeweils zugrunde liegenden
klinischen Datenbasis vor dem Hintergrund der EU-weit harmonisierten Anforderungen an klinische Prüfungen in dieser Indikation... Wird eines
der Arzneimittel, die ausschließlich für die Therapie tiefer Venenthrombosen zugelassen sind, von einem Arzt im Rahmen der ärztlichen
Therapiefreiheit bei Lungenembolie angewendet, so haftet ausschließlich der anwendende Arzt bei eventuellen Schädigungen des Patienten
(Hervorhebung durch Red.). Die Haftung des therapeutischen Unternehmers gemäß § 84ff. Arzneimittelgesetz greift dann nicht.
Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM)
D-53175 Bonn
Enoxaparin (CLEXANE) beispielsweise ist auf der Basis einer Studie mit 900 Thrombosepatienten, in der sich das niedermolekulare Heparin auch bei
vorbestehenden Lungenembolien (knapp ein Drittel der Patienten) nicht von Standardheparin (LIQUEMIN N u.a.) unterscheidet,1 in den USA zur
Behandlung von Lungenembolien zugelassen. Auch in verschiedenen europäischen Ländern ist Enoxaparin für diese Indikation zugelassen.
Hierzulande hat der Hersteller die Zulassung zur Behandlung von Lungenembolien bislang offenbar nicht beantragt.2
In Leitlinien werden fraktionierte Heparine zur Therapie der Lungenembolie alternativ zu unfraktionierten Heparinen empfohlen, ohne dass spezielle Wirkstoffe
benannt werden. Entgegen der vom BfArM dargestellten Auffassung ist die Haftung des Herstellers für ein Arzneimittel nach § 84 ff. AMG nicht auf die
Anwendung bei zugelassenen Indikationen beschränkt, sondern orientiert sich am "bestimmungsgemäßen Gebrauch". Hierzu zählen
auch Off-Label-Verordnungen, sofern sie z.B. in Leitlinien empfohlen werden und der Hersteller dem nicht ausdrücklich widerspricht,3,4 -Red.

|
| © 2004 arznei-telegramm |